1铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体,放出大量的热2铁丝在氧气中燃烧时,为了防止溅落的熔化物炸裂集气瓶底,集气瓶内预留少量水3铁丝在氧气中燃烧生成了四氧化三铁,反应的方程式是3Fe+2O 2 点燃 Fe 3 O 4 ,该反应由两种物质生成了一种物质,属于化合;铁丝在氧气中燃烧生成的四氧化三铁固体温度很高,溅落到集气瓶瓶底时容易把瓶底炸裂,在集气瓶底部先放些水或铺一层细沙的原因是防止溅落的熔化物炸裂集气瓶底故答为防止溅落的熔化物炸裂集气瓶底,点评精心设计实验是实验取得成功的保证,也是不出现安全事故的前提铁丝燃烧集气瓶中水的作用 1硫在氧。
铁在氧气中燃烧的实验现象是铁丝在氧气里剧烈燃烧,火星四溅,产生耀眼的白光,生成黑色固体Fe3O4一此燃烧的反应方程式为3Fe+2O2==点燃==Fe3O4二Fe3O4的性质为黑色晶体黑色,不溶于水,可溶于酸溶液,在自然界中以磁铁矿的形态出现,常温时具有强的亚磁铁性与颇高的导电率;从铁在氧气中燃烧反应中,我们知道这里面产生了一个化合作用,在点燃的条件下,铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁物质 延伸阅读1实验中会出现的火星四射的现象,这是因为在氧气中燃烧时产生气体,比如二氧化碳,推动熔融的铁产生火星四射的现象我们实验用的铁丝不是纯铁,铁丝中含有一。 新奥今天晚上9点35分开特马
不对,铁和氧气反应有几种情况1铁丝在氧气中燃烧生成四氧化三铁 3Fe+2O2=点燃=Fe3O4 2铁丝在潮湿的空气中氧化生成铁锈Fe2O3·nH2O3铁在高温下和氧气反应生成氧化亚铁 2Fe+ O2=高温=2FeO;铁丝在氧气中燃烧的现象剧烈燃烧,火星四射,放热,生成黑色固体实验的注意事项装O2的集气瓶要预先装少量水或瓶底铺上一层细沙,是为了防止溅落的融化物炸裂瓶底铁丝应绕成螺旋状,以增大接触面积铁丝前端系一根火柴,以便引燃铁丝待火柴将要燃尽时,才能将铁丝由上向下缓慢伸入瓶中铁丝上不能。
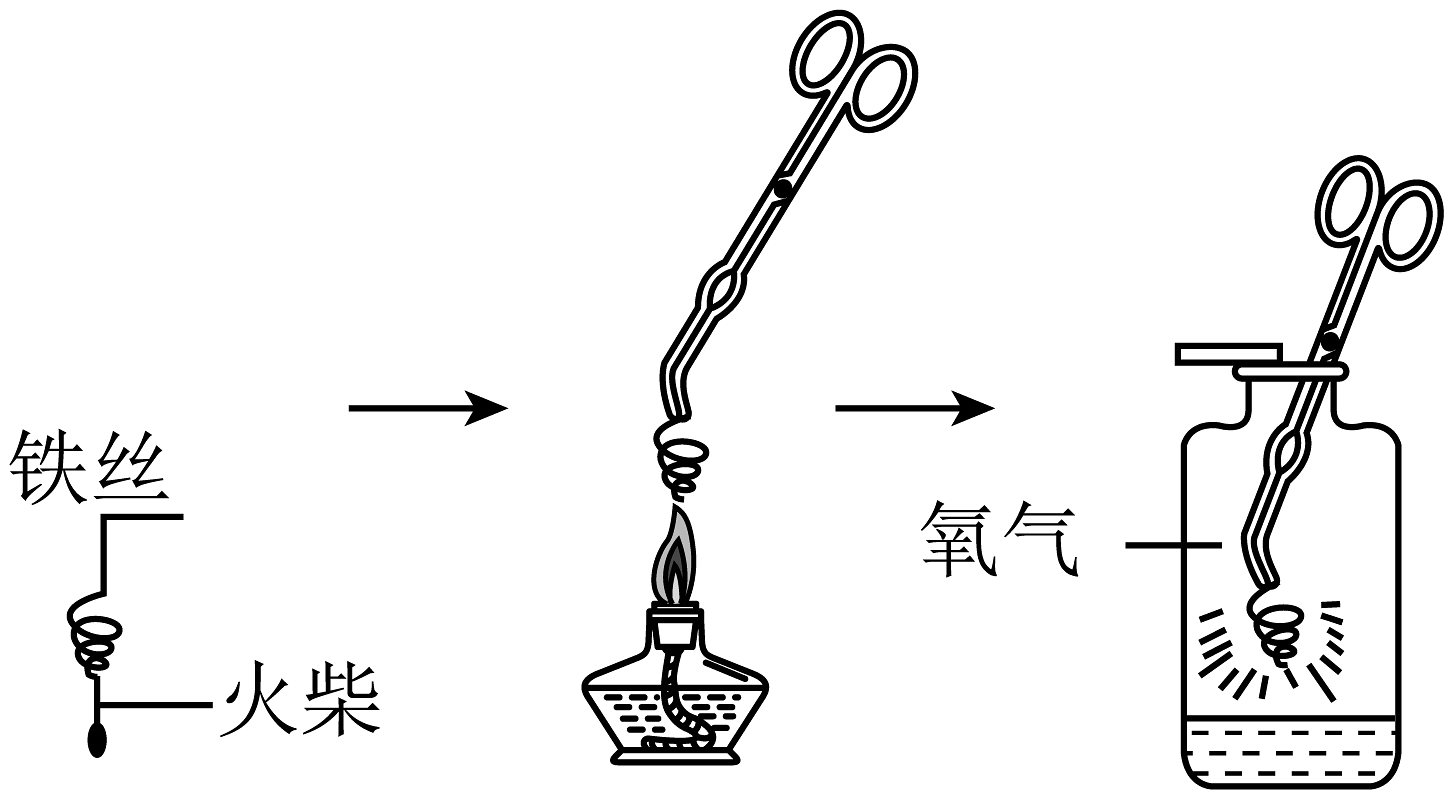
铁丝在氧气中燃烧的现象是?
铁丝在氧气中的燃烧会产生四氧化三铁,化学式为Fe3O4燃烧的化学反应式为3Fe+2O2=点燃=Fe3O4此过程释放大量热量,火焰呈白热状态,且燃烧后铁丝会冷却并变黑在潮湿的空气中,铁丝的氧化反应会生成铁锈,主要化学式为Fe2O3·nH2O此反应通常发生在铁丝表面形成一层红色或棕色的腐蚀层。
1 铁在氧气中燃烧,生成氧化铁当细铁丝在空气中加热至500摄氏度时,在适当的氧过量条件下,会形成四氧化三铁2 铁在高温下与水蒸气反应,产生的产物包括四氧化三铁和氢气这个过程中,氧化亚铁迅速被氧化成四氧化三铁3 在隔绝空气的条件下加热草酸亚铁,可以制备出四氧化三铁4 铁是一。
现象是铁剧烈燃烧火星四射放出热量,而且还会生成黑色的固体注意瓶底要放少量水或细沙,防止生成的固体物质溅落下来,炸裂瓶底会出现的火星四射的现象,这是因为在氧气中燃烧时产生气体,比如二氧化碳,推动熔融的铁产生火星四射的现象铁丝中含有一定数量的碳其实还包括微量的硫磷,碳。
硫在氧气中燃烧,生成有刺激性的气体,发出明亮光铁丝在氧气中剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体木炭在氧气中燃烧,发出白光,放出热量,生成能使澄清石灰水变浑浊的气体红磷在氧气中燃烧,产生大量的白烟,放出热量。
铁丝在氧气中燃烧时火星四射并生成黑色固体的原因如下火星四射这是由于铁丝在氧气中燃烧时,反应非常剧烈,释放出大量的热量这些热量使得铁丝迅速升温并汽化,形成微小的铁颗粒这些铁颗粒在高温下以极高的速度喷射出来,与周围的氧气发生进一步的燃烧反应,从而产生火星四射的现象生成黑色固体铁丝在。
铁丝在氧气中燃烧生成什么物质
1、在高温时,铁在纯氧中燃烧,剧烈反应,火星四射,生成黑色小颗粒的物质,放出大量的热 生成FeO,FeO可以看成是FeO·FeO 铁在氧气中燃烧火星四射的原因是铁丝中通常含有少量碳元素,而纯铁燃烧几乎不会有火星四射的现象化学方程式为3Fe+2O=FeO点燃铁是一种金属元素,原子序数为26,铁单质化学式Fe熔点1538。
2、铁丝在氧气中燃烧的生成物是四氧化三铁铁丝在氧气中燃烧的现象是铁剧烈燃烧火星四射放出热量,而且还会生成黑色的固体氧气除了可以和铁反应外,还能和绝火多数金属起反应除金铂少数几种金属外,例如钠镁等金属加热均能在氧气中燃烧把一根无锈细铁丝弯成螺旋状,一端紧系一段火柴梗。
3、铁丝在氧气中燃烧属于化合反应说明铁丝在氧气中燃烧的反应物是铁和氧气,生成物是四氧化三铁,反应条件是点燃,用最小公倍数法配平,所以方程式是3Fe+2O2==点燃=Fe3O4,属于多变一的反应所以为化合反应化合反应的概念化合反应指的是由两种或两种以上的物质反应生成一种新物质的反应其中。
转载请注明来自中国金属学会,本文标题:《铁丝在氧气中燃烧的现象是?》


 京公网安备11000000000001号
京公网安备11000000000001号 京ICP备11000001号
京ICP备11000001号
还没有评论,来说两句吧...